- 식품품질검사
- 잔류농약분석
- 친환경농산물 안정성분석
- 유기농자재 시험분석
- 유기가공식품인증
- 천연·유기농 화장품 인증
- 유기농 천연 화장품인증(COSMOS)
- 식약처 천연·유기농 화장품 원료 승인
- 의료기기 품질관리 심사
의료기기 품질관리 적합인정
의료기기를 제조 또는 수입하는 업체는 의료기기법 또는 체외진단의료기기법에 따라 반드시 품질관리 적합인정(GMP)을 받은 후에 판매할 수 있습니다. 한국화학융합시험연구원(KTR)은 식품의약품안전처로부터 의료기기 품질심사기관으로 등록되어 GMP 적합 인정 업무를 수행합니다.(품질심사업무범위) 의료기기법, 체외진단의료기기법, 의료기기산업 육성 및 혁신의료기기 지원법에 따른 품질관리체계 심사
의료기기 및 체외진단 의료기기 적용범위
- 의료기기 제조·수입허가 또는 제조·수입인증을 받거나 제조·수입신고를하고자 하는 자
- 임상시험용 의료기기를 제조 또는 수입하고자 하는 자
- 적합성 인정 및 정기심사를 받고자 하는 의료기기 제조업자 또는 수입업자
- ※ 의료기기 제조 및 품질관리기준
- ※ 체외진단 의료기기 제조 및 품질관리기준
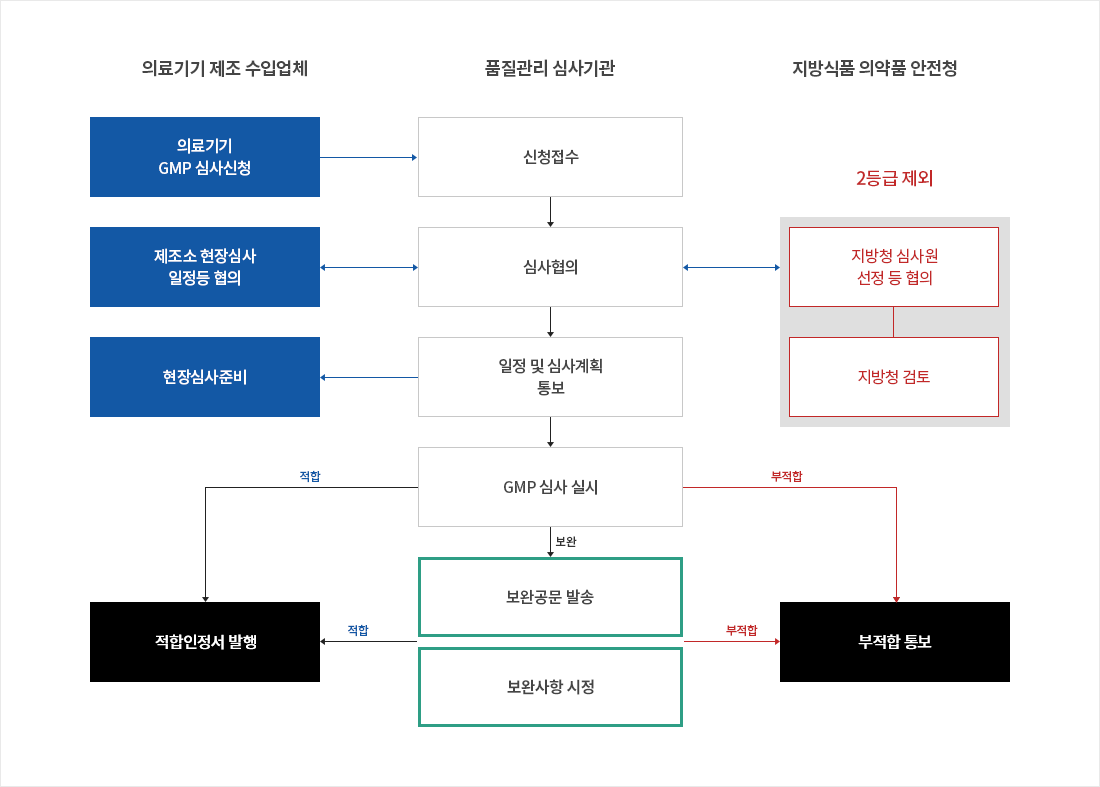
의료기기 GMP 인정업무 처리절차
GMP신청 서식 다운로드
GMP심사 신청 안내수수료
예상 견적 확인(심사 수수료 인상 : 시행 2023.03.01.)
상담업무
- GMP인증팀 대표전화 02-2092-4000
- GMP인증팀 팩스번호 02-2635-6100
- GMP인증팀 대표메일 gmp@ktr.or.kr
관련규정 및 가이드라인 참고자료
의료용구의 품질관리 업무를 담당하고 있는 책임자/담당자들께서는 식양청-의료기기국 홈페이지의 자료실에 업무와 관련한 많은 자료들이 있으므로 참고하시기 바랍니다. 아래 자료들은 의료기기 품질관리 업무 수행에 필요한 자료들이므로 참고하시기 바랍니다.